|
↓
Автор Pavlenko | 28 октября 2010 | Коментарів: 2 | Переглянуто 91167
Рубрика: Уроки колегам біологам / Уроки для 10 класівРозробки уроків до теми "Молекулярний рівень організації життя" 10 кл.
Неорганічні речовини
Урок 1 Елементарний склад живих організмів. Мета. Освітня. Формувати в учнів знання про хімічний склад живих організмів та хімічні процеси, що лежать в основі їхньої життєдіяльності. Ознайомити із органогенними, мікроелементами, мікроелементами та ультрамікроелементами живих організмів. Розглянути біологічну роль хімічних елементів в організмах. Розвиваюча. Розвивати уміння порівнювати значення хімічних елементів у житті організмів та визначати співвідношення цих елементів у живій та неживій природі. Виховна. Виховувати бережливе ставлення до життєвих процесів, які відбуваються в живих організмах та власному організмі. Особливу увагу звернути на ті елементи, нестача яких викликає захворювання живих організмів. Тип уроку. Засвоєння нових знань. Форма уроку. Синтетична. Місце уроку в навчальній темі. Перший у темі . Методи і методичні прийоми: 1. Інформаційно- рецептивний: а) словесний: розповідь-пояснення, опис, бесіда, повідомлення учнів, робота з підручником. б) наочний: ілюстрація, демонстрація, ТЗН. Прийоми навчання: виклад інформації, пояснення, активізація уваги та мислення, одержання з тексту та ілюстрацій нових знань, робота з роздатковим матеріалом. 2. Репродуктивний. Прийоми навчання: подання матеріалу в готовому вигляді, конкретизація і закріплення вже набутих знань. 3. Проблемно - пошуковий: постановка проблемного питання. Прийоми навчання: постановка взаємопов’язаних проблемних запитань, активізація уваги та мислення. 4. Візуальний: складання схематичних малюнків. 5. Релаксопедичний: психологічне розвантаження. Міжпредметні зв ́язки: хімія. Матеріали та обладнання: схеми, малюнки, таблиця Д.Менделєєва. Основні поняття та терміни: біохімія, біогенні елементи, органогенні елементи, мікроелементи, мікроелементи. ХІД УРОКУ І. Актуалізація опорних знань та чуттєвого досвіду учнів. Методом бесіди з’ясувати знання учнів про живу та неживу природу, про склад повітря, основні властивості живого, про рівні організації живого, що таке життя? ІІ. Мотивація навчально-пізнавальної діяльності учнів. Довести: - на основі чого відбувається єдність живої і неживої природи. - чи існує єдність хімічного складу організмів. ІІІ. Сприймання та засвоювання учнями нового матеріалу. Живі і неживі тіла планети побудовані з одних і тих же хімічних елементів. Але в живій природі ці елементи характеризуються складністю хімічних сполук. Це зумовлено певною упорядкованістю їх на молекулярному рівні, тобто відмінності між хімічним складом органічного і неорганічного світу виявляється уже на молекулярному рівні. За дослідженнями біохіміка В.О.Енгельгардта «глибока корінна відміна живого від неживого полягає у здатності живого створювати порядок із хаотичного теплового руху молекул». Хімічні елементи живих організмів створюють два класи сполук – неорганічні і органічні. Із відомих хімічних елементів до складу клітин входить понад 80. Елементів, які були б властиві лише живим організмам, у природі не знайдено. Близько 30 елементів наявні в клітинах постійно, а понад 5 потрапляють водою, їжею, вдихаються. Всі елементи, що входять до складу клітин організмів поділяють на групи: 1. Органогенні – оксисен, нітроген, гідроген, карбон. 2. Макроелементи – кількість їх становить від 0,1% до 0,01 %. 3. Мікроелементи – містяться в кількостях від 0,001% до 0,000001%. 4. Ультрамікроелементи – ті, концентрація яких не перевищує 0, 000001%. Хімічні елементи, які входять до складу клітин і виконують біологічні функції називають біогенними. Всі живі організми відрізняються від навколишньої неорганічної природи за кількісним складом хімічних елементів. Хімічні елементи беруть участь у побудові організму у вигляді іонів. ІV. Осмислення об‘єктивних зв’язків та взаємозалежностей у вивченому матеріалі. Робота над таблицею. 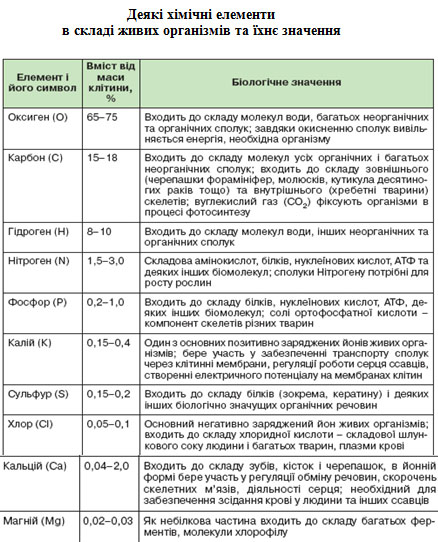  ІV. Осмислення об‘єктивних зв’язків та взаємозалежностей у вивченому матеріалі. V. Узагальнення та систематизація знань. Розглянути колообіг Нітрогену в природі. Дати характеристику. VІ. Підведення підсумків уроку. VІІ. Надання та пояснення домашнього завдання. Поміркувати! Про що свідчить той факт, що в живих організмах не трапляються хімічні елементи, яких не знайдено в неживій природі? Урок 2, 3 Неорганічні речовини: вода і мінеральні солі. Мета. Освітня. Продовжити формувати знання учнів про хімічний склад живих організмів; ознайомити із неорганічними речовинами на прикладі води та мінеральних солей; розкрити біологічний вплив хімічних елементів на організм. Розвиваюча. Розвивати уміння визначати біологічне значення неорганічних сполук як компонентів живих організмів; розвивати увагу, пам’ять, спостережливість. Виховна. Виховувати бережливе ставлення до води як основної рідини нашої планети та живих організмів. Тип уроку. Засвоєння нових знань. Форма уроку. Синтетична. Місце уроку в навчальній темі. Поточний. Методи і методичні прийоми: 1. Інформаційно- рецептивний: а) словесний: розповідь-пояснення, опис, бесіда, повідомлення учнів, робота з підручником. б) наочний: ілюстрація, демонстрація, ТЗН. Прийоми навчання: виклад інформації, пояснення, активізація уваги та мислення, одержання з тексту та ілюстрацій нових знань, робота з роздатковим матеріалом. 2. Репродуктивний. Прийоми навчання: подання матеріалу в готовому вигляді, конкретизація і закріплення вже набутих знань. 3. Проблемно - пошуковий: постановка проблемного питання. Прийоми навчання: постановка взаємопов’язаних проблемних запитань, активізація уваги та мислення. 4.Візуальний: складання схем. 5.Сугестивний: застосування різних видів мистецтва – вірші, музика. 6.Релаксопедичний: психологічне розвантаження. Міжпредметні зв ́язки: хімія, географія. Матеріали та обладнання: схеми, малюнки, таблиці, м\м дошка. Основні поняття та терміни: неорганічні сполуки, неорганічні кислоти, вода, мінеральні солі, гідрофільність, гідрофобність, буферні системи, кислотно-лужний баланс. ХІД УРОКУ І. Актуалізація опорних знань та чуттєвого досвіду учнів. 1. Яка класифікація елементів, що входять до складу живих організмів? 2. Які хімічні елементи можуть нагромаджуватися у деяких рослинах та тваринах? 3. Що таке рослини-розвідники (ті, що допомагають геологам шукати родовища корисних копалин)? 4. Метали чи неметали переважають у живих організмах? 5. Характеристика деяких хімічних елементів, що входять до складу живих організмів? ІІ. Мотивація навчально-пізнавальної діяльності учнів. 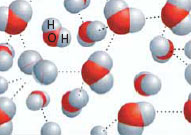 Проблемні запитання. - Чому вода має першочергове значення у клітинах живих організмів? - Чи можлива нормальна життєдіяльність організму без мінеральних солей? - Чи залежить кількість води та мінеральних солей від вікових категорій людей? ІІІ. Сприймання та засвоювання учнями нового матеріалу. Вода утворює основу внутрішнього середовища організмів: цитоплазма, кров, лімфа, тканинна рідина, рослинний сік… Вміст води в організмах становить 60–70 %, а в деяких випадках – до 98 %. Цитоплазма більшості клітин містить приблизно 80 % води. Кров і лімфа людини містять понад 80 % води. Воді притаманні унікальні хімічні й фізичні властивості. молекула води складається з двох атомів Гідрогену, сполучених з атомом Оксигену ковалентними зв’язками. На полюсах молекули води розміщені позитивні і негативний заряди, тобто вона полярна. Завдяки цьому дві сусідні молекули зазвичай взаємно притягуються за рахунок сил електростатичної взаємодії між негативним зарядом атома Оксигену однієї молекули та позитивним зарядом атома Гідрогену іншої. При цьому виникає водневий зв’язок, у 15–20 разів слабший за ковалентний. Коли вода перебуває в рідкому стані, її молекули безперервно рухаються і водневі зв’язки постійно то розриваються, то виникають знову. Частина молекул води формує водну оболонку навколо деяких сполук (наприклад, білків). Таку воду називають зв’язаною, або структурованою (4–5 % загальної кількості води в організмах). Структурована вода, що формує водну оболонку навколо певних молекул, запобігає їхній взаємодії. Крім того, вода бере участь у підтриманні структури певних молекул, наприклад білків. Решта 95–96 % води має назву вільної: вона не пов’язана з іншими сполуками. Залежно від температури середовища вода здатна змінювати агрегатний стан. За зниження температури вода з рідкого стану може переходити в твердий, а за підвищення – у газуватий. Від концентрації йонів Гідрогену, яку оцінюють за водневим показником (рН – значення негативного десяткового логарифма концентрації йонів Н+), залежать структурні особливості та активність макромолекул. Нейтральній реакції розчину відповідає рН 7,0. Якщо його значення нижче – реакція розчину кисла, вище – лужна. Водні розчини, здатні протистояти зміні їхнього показника рН при додаванні певної кількості кислоти або лугу, називають буферними системами. Вони складаються зі слабкої кислоти (донора Н+) і основи (акцептора Н+), здатних відповідно зв’язувати йони гідроксилу (ОН–) та Гідрогену (Н+), завдяки чому рН усередині клітини майже не змінюється. По відношенню до води всі речовини в природі поділяються на дві групи: гідрофільні – добре розчинні у воді та гідрофобні – практично нерозчинні у воді. Водний баланс людини. Вміст води в організмі людини становить близько 65 %. Тобто, якщо маса людини становить 60 кг, то з них 39 кг припадає на воду. Вміст води залежить і від віку: у новонароджених він становить близько 75–80 %, у період завершення росту – 65–70 %, а в людей похилого віку – лише 55–60%. Між різними органами і тканинами людини вода розподілена нерівномірно: найбільше її в крові та нирках – 82–83 %, головному мозку – до 80 %, печінці – 75 %, м’язах – 70–76 %, у жировій тканині – близько 30 %, кістках – близько 20 %. 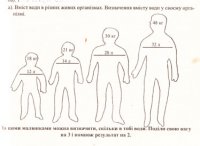 Оскільки організм людини щоденно витрачає приблизно 2–2,5л води (вона виводиться з неперетравленими рештками їжі, сечею, потом, випаровується з поверхні слизових оболонок ротової порожнини та дихальних шляхів), то така сама її кількість має постійно надходити туди. Шляхи надходження води до організму різні. Крім того, близько 1 л води потрапляє з продуктами харчування, ще майже 300 мл води утворюється внаслідок окиснення жирів, білків і вуглеводів (так звана метаболічна вода). Кількість спожитої за добу води залежить від умов, у яких перебуває людина. Солі неорганічних кислот усередині живих організмів розчинені у воді (у вигляді йонів) або перебувають у твердому стані (наприклад, солі Кальцію та Фосфору у складі скелета людини та більшості хребетних тварин). Йони утворені катіонами металічних елементів (Калію, Натрію, Кальцію, Магнію тощо) та аніонами неорганічних кислот (Cl–, HSO4–, SO42–,НСО3–, Н2РО4–, НРО42– та ін.). Різна концентрація йонів Na+ і К+ поза клітинами та всередині них приводить до виникнення різниці електричних потенціалів на мембранах, які оточують клітини. Це забезпечує транспорт речовин через мембрани, а також передачу нервових імпульсів. До складу багатьох ферментів входять йони Са2+ і Mg2+, які забезпечують їхню активність. Присутність у плазмі крові йонів Са2+ – необхідна умова зсідання крові. За нестачі солей Кальцію порушується робота серцевого та скелетних м’язів (зокрема, виникають судоми). Сталий уміст натрій хлориду (0,9 %) у плазмі крові – необхідна складова підтримання гомеостазу нашого організму. Розчин натрій хлориду такої концентрації ще називають фізіологічним. Його використовують при ін’єкціях певних ліків або вводять за незначних крововтрат. Важливі функції виконують в організмі і неорганічні кислоти. Наприклад, хлоридна кислота створює кисле середовище в шлунку хребетних тварин і людини, забезпечуючи активність ферментів шлункового соку. У людей, в шлунку яких хлоридної кислоти виробляється недостатня кількість, порушуються процеси перетравлення білків, можливе розмноження у шлунку великої кількості шкідливих бактерій тощо. Збільшення секреції хлоридної кислоти також небезпечне для організму людини, зокрема воно спричиняє печію. Залишки сульфатної кислоти, приєднуючись до нерозчинних у воді сполук, забезпечують їхню розчинність. Це сприяє виведенню таких речовин у розчиненому стані з клітин і організму. Ортофосфатна кислота необхідна для синтезу АТФ (є універсальним накопичувачем енергії в клітині) та різних типів нуклеїнових кислот. Кислотно-лужний баланс. Внутрішнє середовище людини має певне співвідношення позитивних і негативних йонів – кислотно-лужний баланс. У разі його порушення можуть виникати важкі захворювання. Зокрема, при підвищенні вмісту позитивних йонів організм погано засвоює Кальцій, Натрій, Калій, а при зростанні вмісту негативних – повільніше засвоюється їжа, що негативно впливає на функції печінки і нирок, виникають алергічні стани, загострюються хронічні захворювання. Загальний вміст неорганічних речовин (крім води) у клітинах різних типів варіює в межах від одного до декількох відсотків. Серед цих сполук важливу роль у забезпеченні нормального функціонування окремих клітин і цілісних організмів відіграють кислоти, луги та солі. ІV. Осмислення об‘єктивних зв’язків та взаємозалежностей у вивченому матеріалі. Функції води в організмах.  1. Збереження об’єму клітин організмів. 2. Створення пружності клітин (тургор). 3. Універсальний розчинник. 4. Середовище, де відбуваються хімічні реакції. 5. Безпосередня участь в хімічних реакціях. 6. Забезпечення рівномірного розподілу тепла в організмі. 7. Створення водного балансу організму. 8. Захист організму від коливань температури. 9. Змащувальний матеріал в органах. 10. Забезпечення транспорту речовин (поживних, продуктів обміну). V. Узагальнення та систематизація знань. VІ. Підведення підсумків уроку. Воді належить першочергова роль у забезпеченні функціонування окремих клітин, органів та цілісних організмів. VІІ. Надання та пояснення домашнього завдання. Приготувати повідомлення про: - радіонукліди; - ізотопи; - Вимоги до питної води та її якості. Органічні речовини Урок 1 Малі органічні молекули: ліпіди, моносахариди, їхня будова, властивості, функції. Лабораторна робота № 1 «Визначення деяких органічних речовин та їхніх властивостей» Мета. Освітня. Розширити знання учнів про хімічний склад живих організмів, а саме про органічні сполуки; ознайомити із будовою, властивостями та функціями ліпідів та вуглеводів, (моносахаридів); розкрити значення цих органічних сполук у живій природі. Розвиваюча. Розвивати уміння порівнювати будову та функції органічних молекул та сполук у клітинах живих організмів; уміння спостерігати, аналізувати та робити відповідні висновки. Виховна. Виховувати матеріалістичні погляди та уявлення про спадковий зв’язок живої і неживої природи, про єдність хімічного складу організмів. Тип уроку. Засвоєння нових знань. Форма уроку. Синтетична. Місце уроку в навчальній темі. Поточний. Методи і методичні прийоми: 1. Інформаційно- рецептивний: а) словесний: розповідь-пояснення, опис, бесіда, повідомлення учнів, робота з підручником. б) наочний: ілюстрація, демонстрація. в) практичний: виконання лабораторної роботи. Прийоми навчання: виклад інформації, пояснення, активізація уваги та мислення, одержання з тексту та ілюстрацій нових знань. 2. Репродуктивний. Прийоми навчання: подання матеріалу в готовому вигляді, конкретизація і закріплення вже набутих знань. 3. Проблемно - пошуковий: постановка проблемного питання. Прийоми навчання: постановка взаємопов’язаних проблемних запитань, активізація уваги та мислення. 5. Релаксопедичний: психологічне розвантаження. Міжпредметні зв ́язки: хімія, фізика, географія. Матеріали та обладнання: схеми, малюнки, таблиці. Основні поняття та терміни: органічні сполуки, малі органічні молекули, ліпіди, жири, фосфоліпіди, гліцерин, жирні кислоти: олеїнова, пальмітинова, стеаринова; мікромолекули, макромолекули, біополімери, мономери. ХІД УРОКУ І. Актуалізація опорних знань та чуттєвого досвіду учнів. Повторити знання учнів про неорганічні сполуки: - будова молекули води; - функції води у клітині; - значення мінеральних солей. Із переліку хімічних елементів C, Cl, I, K, F, Mg, P, Ca, O, Na вибрати один згідно запитань: - входить до складу біомолекул; С - основний позитивно заряджений іон в організмі тварин; К - основний компонент кісток і черепашок; Са - негативно заряджений іон в організмі тварин; Cl - головний внутрішньоклітинний позитивно заряджений іон; Na - входить до складу гормонів щитовидної залози; I - входить до складу зубів; F - структурний елемент білків, нуклеїнових кислот, АТФ; Р - активізує діяльність ферментів, структурний компонент хлорофілу; Mg - входить до складу води та біомолекул; О. Повідомлення учнів про значення неорганічних речовин для життєдіяльності різних організмів. ІІ. Мотивація навчально-пізнавальної діяльності учнів. Ми повинні розширити знання про хімічні сполуки живих організмів, про їхні властивості та значення у клітинах. ІІІ. Сприймання та засвоювання учнями нового матеріалу. Органічні речовини – це сполуки Карбону з іншими елементами, що виникли в живих істотах або є продуктами їхньої життєдіяльності. Органічні сполуки присутні в атмосфері, поверхневих і підземних водах, осадах, ґрунтах і гірських породах. У складі органічних сполук переважають органогенні хімічні елементи (Гідроген, Оксиген, Нітроген і Карбон). Ковалентно зв’язані атоми Карбону утворюють ланцюжки або ряди кілець (так званий скелет молекули). До складу клітин входять різні органічні сполуки: ліпіди, вуглеводи, білки, нуклеїнові кислоти тощо. Їхні молекули можуть мати високу молекулярну масу. Зокрема, молекулярна маса більшості білків становить від 6000 до 1 000 000, деяких нуклеїнових кислот – сягає кількох мільярдів дальтонів (1 дальтон відповідає 1/12 атомної маси ізотопу карбону 12С, тобто 1,67•10-24 г). Високомолекулярні органічні сполуки можуть складатися з великої кількості однакових чи різних за хімічною будовою ланок (простих молекул – мономерів). Такі сполуки називають біополімерами, або макромолекулами. Наприклад, молекули білків складаються із залишків амінокислот, нуклеїнових кислот – з нуклеотидів, а складних вуглеводів (полісахаридів) – з моносахаридів. Ліпіди – це низькомолекулярні речовини з гідрофобними властивостями. Вони нерозчинні у воді, але добре розчинні в органічних розчинниках: ефірі, бензині, хлороформі. У різних органах і тканинах вміст ліпідів неоднаковий: дуже багато їх у нервовій тканині, печінці, серці, нирках, насінні, плодах… За хімічною будовою – це складні сполуки трьохатомного спирту гліцерину і високомолекулярних жирних кислот: пальмітинової, стеаринової, олеїнової. Всі жирні кислоти поділяються на насичені і ненасичені. На сьогодні всі ліпіди поділяються на нейтральні – жири і жироподібні речовини - ліпоїди (віск, фосфоліпіди, ліпопротеїди, гліколіпіди, терпени, стероїди). 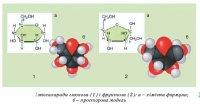 Різноманітність ліпідів. Серед ліпідів розрізняють прості та складні. До простих ліпідів належать речовини, які побудовані зі сполучених між собою залишків жирних кислот (або альдегідів) і спиртів, наприклад жири та воски. Складні ліпіди – сполуки, утворені внаслідок взаємодії молекул простих ліпідів з іншими речовинами. До них належать ліпопротеїди (сполуки ліпідів і білків), гліколіпіди (ліпідів і вуглеводів), фосфоліпіди (ліпідів і ор- тофосфатної кислоти). Жири – складні естери, утворені триатомним спиртом гліцерином і трьома залишками жирних кислот. Вони відкладаються у вигляді жирових включень у рослинних і тваринних клітинах. Підвищений вміст жирів (до 90%) характерний для клітин нирок, підшкірної клітковини, жовтого тіла членистоногих. У деяких рослин (соняшника, волоського горіха, маслин) жирів багато в насінні та плодах. Воски виконують здебільшого захисну функцію. У ссавців віск виділяють лоєві залози шкіри: вони надають шкірі еластичності і зменшують зношення волосяного покриву. У птахів віск секретує куприкова залоза, розташована над основою хвоста. Її секрет надає пір’яному покриву водовідштовхувальних властивостей (пригадайте: ця залоза добре розвинена саме у водоплавних птахів). Восковий шар вкриває листки наземних рослин і поверхню зовнішнього скелета членистоногих – мешканців суходолу, запобігаючи надлишковому випаровуванню води з поверхні тіла. Добре розвинені восковидільні залози, розташовані в черевці медоносних бджіл-робітниць. Як ви пам’ятаєте, з воску бджоли будують стільники. Віск широко використовують у медицині, промисловості та інших сферах діяльності людини. Ще одна важлива група ліпідів – гідрофобні спирти стероїди. Карбоновий ланцюжок стероїдів утворює декілька кілець, тому вони належать до так званих циклічних органічних сполук. Стероїдну природу, зокрема, мають статеві гормони людини – естрогени (жіночі) та андрогени (чоловічі), а також гормони надниркових залоз (кортикостероїди). Один з найвідоміших стероїдів – холестерин. В організмі ссавців і людини він слугує попередником під час синтезу статевих гормонів. У плазмі крові холестерин перебуває у вигляді складних естерів з жирними кислотами, які він транспортує. Холестерин синтезують клітини печінки; Вуглеводи – органічні речовини, до складу яких входять С, О, Н. Загальна формула Сn (Н2О)n. Всі вуглеводи поділяються на моносахариди і полісахариди. Моносахариди – прості цукри, що складаються з однієї молекули і являють собою тверді, кристалічні речовини, розчинні у воді і солодкі на смак. У залежності від кількості вуглецевих атомів, що входять до молекули вуглецю, розрізняють:  - триози – мають 3 атоми; - тетрози – 4 атоми; - пентоди – 5 атомів; - гексози – 6 атомів. Моносахариди здебільшого мають загальну формулу СnH2nOn. Вони можуть містити від 3 до 10 атомів Карбону: тріози (3 атоми Карбону), тетрози (4), пентози (5), гексози (6) і так далі до декози (10). У природі найпоширеніші гексози та пентози. Прикладами гексоз є глюкоза, фруктоза. Ці сполуки надають солодкого смаку плодам, меду, а глюкоза є дуже важливою складовою метаболізму. До пентоз, наприклад, належать рибоза і дезоксирибоза, що входять до складу відповідно рибонуклеїнових (РНК) і дезоксирибонуклеїнової (ДНК) кислот. Моносахариди добре розчиняються у воді. ІV. Осмислення об‘єктивних зв’язків та взаємозалежностей у вивченому матеріалі. Виконання лабораторної роботи “Виявлення деяких органічних молекул та їхніх властивостей”. V. Узагальнення та систематизація знань. Доповнити схему. 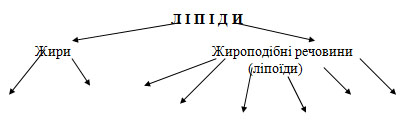 Значення ліпідів: - структурна функція; - енергетична функція (1 г ліпідів дає 38,9 кДж енергії); - теплоізоляційна; - запасаюча; - джерело ендогенної води (при окисленні 100 г жиру утворюється 107 мл води); - функція захисту (навколониркова капсула, жирові подушки навколо органів); - регуляторна функція (гормони – естрадіол, тестостерон). VІ. Підведення підсумків уроку. VІІ. Надання та пояснення домашнього завдання. Урок 2 Малі органічні молекули: амінокислоти, нуклеотиди, їхня будова, властивості, функції. Мета. Освітня. Розширити знання учнів про біополімери; ознайомити із будовою, властивостями та функціями амінокислот та нуклеотидів як мономерів складних органічних сполук. Розвиваюча. Розвивати уміння порівнювати органічні сполуки та їхнє значення у життєдіяльності організмів, уміння спостерігати, співставляти та робити відповідні висновки. Виховна. Виховувати бережливе ставлення до живих організмів планети. Тип уроку. Засвоєння нових знань. Форма уроку. Синтетична. Місце уроку в навчальній темі. Поточний. Методи і методичні прийоми: 1. Інформаційно- рецептивний: а) словесний: розповідь-пояснення, опис, бесіда, повідомлення учнів, робота з підручником. б) наочний: ілюстрація, демонстрація, ТЗН. Прийоми навчання: виклад інформації, пояснення, активізація уваги та мислення, одержання з тексту та ілюстрацій нових знань, робота з роздатковим матеріалом. 2. Репродуктивний. Прийоми навчання: подання матеріалу в готовому вигляді, конкретизація і закріплення вже набутих знань. 3. Проблемно - пошуковий: постановка проблемного питання. Прийоми навчання: постановка взаємопов’язаних проблемних запитань, активізація уваги та мислення. 4.Візуальний: складання схем. 5.Сугестивний: застосування різних видів мистецтва – вірші. 6.Релаксопедичний: психологічне розвантаження. Міжпредметні зв ́язки: хімія, історія. Матеріали та обладнання: схеми, малюнки, таблиці. Основні поняття та терміни: біополімери, мономери, пептид, дипептид, поліпептид, амінокислоти, нуклеотиди. ХІД УРОКУ І. Актуалізація опорних знань та чуттєвого досвіду учнів. Біологічний диктант. 1. Більше вуглеводів міститься у тваринних чи рослинних клітинах? (у рослинних) 2. Полісахариди добре чи погано розчинні у воді? (погано) 3. До біологічних функцій вуглеводів належать ………….. . 4. В основі енергетичної функції ліпідів лежать гідрофобність, погана теплопровідність чи розщеплення на простіші речовини?(розщеплення) 5. Якщо взяти дві речовини: рибозу і лецитин, то яким із способів точно можна встановити де що: а) за запахом; б) за розчинністю у воді;+ в) за кольором. ІІ. Мотивація навчально-пізнавальної діяльності учнів. Повідомити тему, мету та завдання уроку. Поміркувати над словами Й.Гете «Щоб освоїти безконечне, треба роз’єднати, а потім сполучити». ІІІ. Сприймання та засвоювання учнями нового матеріалу. Білки – високомолекулярні нітрогеновмісні біополімери, мономерами яких є залишки амінокислот. Амінокислоти – це органічні кислоти, що містять аміногрупу (–NH2), якій притаманні лужні властивості, та карбоксильну групу (–СООН) з кислотними властивостями. Ці групи, як і атом Гідрогену, зв’язані з одним і тим самим атомом Карбону. Є у складі амінокислот й специфічні для кожної з них частини. Їх називають радикалами (R-групами). Загалом у тканинах живих істот трапляється понад 100 амінокислот, але до складу білків входять лише 20 основних, які зустрічаються майже в усіх білках. Крім того, неосновні амінокислоти, кожна з яких – похідна однієї з основних, є компонентами лише окремих типів білків. Наприклад, білок колаген, який входить до складу сполучної тканини, містить гідроксипролін (похідну амінокислоти проліну); у протромбіні (одному з білків, які відповідають за процес зсідання крові) знайдено карбоксиглутаміно- ву кислоту (похідну глутамінової кислоти) тощо. Різні комбінації лише 20 амінокислот забезпечують нескінченну різноманітність білкових молекул (число можливих варіантів – близько 2 • 1018). Зокрема, в організмі людини трапляється понад 5 млн. типів білкових молекул. Молекула кожного певного білка характеризується специфічними складом і послідовністю амінокислотних залишків, які надають їй неповторних функціональних властивостей. Існують різні класифікації амінокислот. Зокрема, амінокислоти поділяють на замінні та незамінні. Замінні амінокислоти організму людини і тварин здатні синтезуватися з продуктів обміну речовин. Натомість, незамінні амінокислоти в організмах людини і тварин не утворюються, а надходять разом з їжею. Ці амінокислоти синтезують рослини, гриби, бактерії. Білки, які містять усі незамінні амінокислоти, називають повноцінними, на відміну від неповноцінних, до складу яких не входять окремі незамінні амінокислоти. Слід зазначити, що для різних видів тварин і людини набір незамінних амінокислот неоднаковий, до того ж він може змінюватися з віком. Наприклад, аргінін або гістидин – замінні для дорослих і незамінні для дітей. Відсутність або нестача однієї чи кількох незамінних амінокислот спричиняють негативний баланс Нітрогену в організмі, порушення біосинтезу білків, гальмування росту й розвитку. Залишки молекул амінокислот у складі білків сполучені між собою міцним ковалентним зв’язком, який виникає між карбоксильною групою однієї амінокислоти та аміногрупою іншої. Цей тип зв’язку називають пептидним (від грец. пептос - зварений). Завдяки такому міцному зв’язку утворюється сполука, яка складається із залишків двох амінокислот – дипептид. Структури, які складаються з великої кількості залишків амінокислот (від 6–10 до декількох десятків), належать дополіпептидів. Нуклеїнові кислоти – складні високомолекулярні біополімери, мономерами яких є нуклеотиди. Молекула нуклеотиду складається з трьох частин: залишків нітратної основи, п’ятивуглецевого моносахариду (пентози) та ортофосфатної кислоти. Залежно від виду пентози, що входить до складу нуклеотиду, розрізняють два типи нуклеїнових кислот: дезоксирибонуклеїнову (ДНК) і рибонуклеїнові (РНК). До складу ДНК входить залишок дезоксирибози, а РНК – рибози. ІV. Осмислення об‘єктивних зв’язків та взаємозалежностей у вивченому матеріалі. Робота над таблицею скорочених назв амінокислот 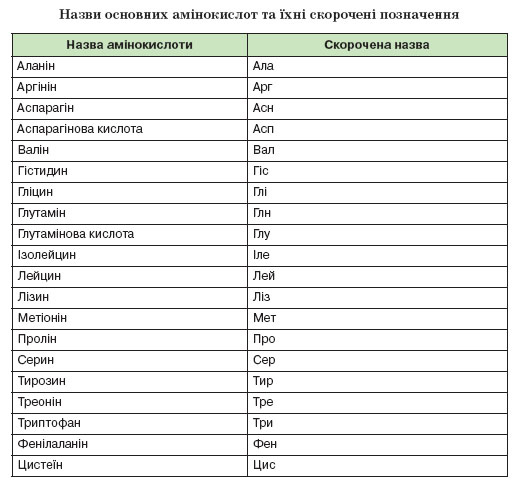 V. Узагальнення та систематизація знань. 1. Яка будова амінокислот, поліпептидів та білків? 2. Які амінокислоти називають замінними та незамінними? 3. Як амінокислоти сполучаються в поліпептидний ланцюг? VІ. Підведення підсумків уроку. VІІ. Надання та пояснення домашнього завдання. Урок 3 Макромолекули: полісахариди, білки, їхня будова, властивості, функції. Лабораторна робота № 2 «Вивчення властивостей ферментів» Мета. Освітня. Сформувати знання учнів про природні полімери; ознайомити із будовою, властивостями і функціями полісахаридів та білків; розкрити значення цих органічних сполук у живій природі. Розвиваюча. Розвивати уміння порівнювати будову та функції органічних молекул та сполук у клітинах живих організмів; уміння спостерігати, аналізувати та робити відповідні висновки. Виховна. Виховувати матеріалістичні погляди та уявлення про спадковий зв’язок живої і неживої природи на основі єдності хімічного складу. Тип уроку. Засвоєння нових знань. Форма уроку. Синтетична. Місце уроку в навчальній темі. Поточний. Методи і методичні прийоми: 1. Інформаційно- рецептивний: а) словесний: розповідь-пояснення, опис, бесіда, повідомлення учнів, робота з підручником. б) наочний: ілюстрація, демонстрація; в) практичний: виконання лабораторної роботи. Прийоми навчання: виклад інформації, пояснення, активізація уваги та мислення, одержання з тексту та ілюстрацій нових знань. 2. Репродуктивний. Прийоми навчання: подання матеріалу в готовому вигляді, конкретизація і закріплення вже набутих знань. 3. Проблемно - пошуковий: постановка проблемного питання. Прийоми навчання: постановка взаємопов’язаних проблемних запитань, активізація уваги та мислення. 4.Релаксопедичний: психологічне розвантаження. Міжпредметні зв ́язки: хімія, фізика, географія. Матеріали та обладнання: схеми, малюнки, таблиці. Основні поняття та терміни: органічні сполуки, полімери, біополімери, мономери, білки, ферменти, амінокислоти, рівні організації білкової молекули. ХІД УРОКУ І. Актуалізація опорних знань та чуттєвого досвіду учнів. 1. З’ясувати знання учнів про вуглеводи. Про які сполуки йде мова? - малі молекули, що легко розчиняються у воді і солодкі на смак? (моносахариди); - солодкі на смак, кристалізуються, легко розчиняються? (дисахариди). 2. Пояснити функції вуглеводів: - енергетична; структурна; опорна; запасна; захисна. 3. За рахунок чого до складу живих організмів входить 2×1018 видів білків? ІІ. Мотивація навчально-пізнавальної діяльності учнів. Повідомити тему, мету та завдання уроку. ІІІ. Сприймання та засвоювання учнями нового матеріалу. Розповідь про полісахариди. Олігосахариди – полімерні вуглеводи, в яких 2–10 моносахаридних ланок з’єднані ковалентними (глікозидними) зв’язками. Зокрема, дисахариди утворені сполученням залишків двох молекул моносахаридів. Приклади дисахаридів: мальтоза (солодовий цукор) – складається з двох залишків глюкози; сахароза (буряковий або тростинний цукор) – складається із залишків глюкози і фруктози; лактоза (молочний цукор) – складається з глюкози та галактози; трегалоза (грибний цукор) – складається з двох залишків глюкози. Вони мають солодкий смак і добре розчиняються у воді.  Полісахариди – це біополімери, молекулярна маса деяких з них може сягати кількох мільйонів. Полісахариди відрізняються один від одного не тільки складом мономерів, а й довжиною та ступенем розгалуженості ланцюгів. Одні полісахариди складаються із залишків одного й того самого моносахариду, інші – різних. Приклади полісахаридів: крохмаль, целюлоза, глікоген, пектин, лігнін, хітин та ін. Вони майже не розчиняються у воді і не мають солодкого присмаку. Вуглеводи можуть вступати у зв’язок з іншими сполуками. Такі вуглеводи називають складними. Приклади: глікопротеїди (сполуки вуглеводів з білками), гліколіпіди (сполуки вуглеводів з ліпідами). Функції вуглеводів досить різноманітні (енергетична, резервна, будівельна, транспортна, захисна). - Енергетична функція. При розщепленні 1 г полісахаридів або олігосахаридів до моносахаридів виділяється 17,6 кДж теплової енергії. Вуглеводи відіграють провідну роль в енергетичному обміні: вони здатні як до окиснення, так і до розщеплення у безкисневих умовах. Це надзвичайно важливо для організмів, які мешкають в умовах дефіциту кисню (наприклад, паразити внутрішніх органів людини і тварин) або за його повної відсутності (анаероби, як-от дріжджі, деякі види бактерій). - Резервна функція. Полісахариди можуть відкладатись у клітинах про запас, найчастіше у вигляді зерен. У клітинах рослин накопичується крохмаль, тварин і грибів – глікоген (мал. 8.3). Ці запасні сполуки є резервом поживних речовин. - Будівельна (структурна) функція вуглеводів полягає в тому, що полісахариди входять до складу певних структур. Так, нітрогеновмісний полісахарид хітин міститься у зовнішньому скелеті членистоногих і клітинній стінці грибів; клітинні стінки рослин утворені з целюлози. До складу надмембранних структур клітин тварин (глікокаліксу) і прокаріотів (клітинної стінки) входять вуглеводи, пов’язані з білками та ліпідами. Ці сполуки забезпечують з’єднання клітин між собою. Особливі сполуки вуглеводів з білками (мукополісахариди) виконують в організмах хребетних тварин і людини функцію мастила, входячи до складу рідини, що змащує суглобові поверхні. - Захисна функція. Полісахариди пектини здатні зв’язувати деякі токсини та радіонукліди, запобігаючи потраплянню їх у кров. Мукополісахарид гепарин запобігає зсіданню крові, підвищує проникність судин, стійкість організму до нестачі кисню (гіпоксії), впливу вірусів і токсинів, знижує рівень концентрації цукру у крові. Розповідь про білки. Серед усіх речовин органічної природи білки займають особливе місце – вони становлять основу структури всіх живих систем і виконують ряд важливих функцій. Рівні просторової організації білків. Відомо чотири рівні просторової організації, або конформації, білків: первинний, вторинний, третинний і четвертинний. Первинну структуру білків визначає певна послідовність амінокислотних залишків, з’єднаних за допомогою пептидних зв’язків. Саме первинна структура і визначає властивості та функції тієї чи іншої білкової молекули. Часто молекула білка у вигляді такого ланцюга не придатна до виконання свого призначення. Для цього вона, наприклад, має повністю або частково закрутитися у спіраль, тобто набути вторинної структури завдяки водневим зв’язкам. Такі зв’язки виникають між атомами Гідрогену NH-групи одного витка спіралі та Оксигену СО-групи іншого витка спіралі. 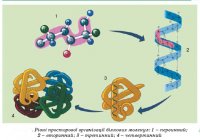 Хоча ці зв’язки значно слабші за пептидні, однак разом вони формують досить міцну структуру. Третинна структура зумовлена здатністю поліпептидної спіралі закручуватися певним чином у грудку, або глобулу, завдяки зв’язкам, які виникають між залишками амінокислоти цистеїну (так звані дисульфідні зв’язки). Підтримання третинної структури забезпечують гідрофобні, електростатичні та інші взаємодії, а також водневі зв’язки. Гідрофобні взаємодії – це сили тяжіння між неполярними молекулами або між неполярними ділянками молекул у водному середовищі. Гідрофобні залишки усяких амінокислот у водному розчині зближуються, наче «злипаються», та стабілізують структуру білка. Електростатичні зв’язки виникають між негативно та позитивно зарядженими радикалами залишками амінокислот. Четвертинна структура білків виникає, коли об’єднуються кілька глобул. Наприклад, молекула гемоглобіну складається з чотирьох залишків молекул білка міоглобіну. Залежно від хімічного складу білки поділяють на прості та складні. Прості, або протеїни, складаються лише з амінокислотних залишків, а складні, або протеїди, у молекулах містять також небілкові компоненти – залишки ортофосфатної та нуклеїнових кислот, вуглеводів, ліпідів, атоми Феруму, Цинку, Купруму тощо. Складні білки називають глікопро теїдами (сполуки з вуглеводами), ліпопротеїдами (з ліпідами), нуклеопротеїдами (з нуклеїновими кислотами) тощо. Багато білків утворюють складні комплекси з пігментами – забарвленими у різні кольори органічними сполуками. Хоча ці зв’язки значно слабші за пептидні, однак разом вони формують досить міцну структуру. Третинна структура зумовлена здатністю поліпептидної спіралі закручуватися певним чином у грудку, або глобулу, завдяки зв’язкам, які виникають між залишками амінокислоти цистеїну (так звані дисульфідні зв’язки). Підтримання третинної структури забезпечують гідрофобні, електростатичні та інші взаємодії, а також водневі зв’язки. Гідрофобні взаємодії – це сили тяжіння між неполярними молекулами або між неполярними ділянками молекул у водному середовищі. Гідрофобні залишки усяких амінокислот у водному розчині зближуються, наче «злипаються», та стабілізують структуру білка. Електростатичні зв’язки виникають між негативно та позитивно зарядженими радикалами залишками амінокислот. Четвертинна структура білків виникає, коли об’єднуються кілька глобул. Наприклад, молекула гемоглобіну складається з чотирьох залишків молекул білка міоглобіну. Залежно від хімічного складу білки поділяють на прості та складні. Прості, або протеїни, складаються лише з амінокислотних залишків, а складні, або протеїди, у молекулах містять також небілкові компоненти – залишки ортофосфатної та нуклеїнових кислот, вуглеводів, ліпідів, атоми Феруму, Цинку, Купруму тощо. Складні білки називають глікопро теїдами (сполуки з вуглеводами), ліпопротеїдами (з ліпідами), нуклеопротеїдами (з нуклеїновими кислотами) тощо. Багато білків утворюють складні комплекси з пігментами – забарвленими у різні кольори органічними сполуками.Властивості білків. Функціональні властивості білків зумовлені їхнім амінокислотним складом і просторовою структурою. За формою молекул розрізняють фібрилярні (ниткоподібні) та глобулярні (кулясті) білки. Фібрилярні білки зазвичай нерозчинні у воді й виконують структурну (наприклад, кератин входить до складу волосся людини або шерсті тварин) або рухову (м’язові білки) функції. Натомість глобулярні білки здебільшого водорозчинні та виконують інші функції: наприклад, гемоглобін забезпечує транспорт газів, пепсин – розщеплення білків їжі, імуноглобуліни (антитіла) – захисну. Глобулярні білки менш стійкі (пригадайте з власного досвіду: білок курячих яєць навіть за незначного підвищення температури легко змінює свою структуру). Одна з основних властивостей білків – їхня здатність під впливом різних чинників (дія концентрованих кислот і лугів, важких металів, високої температури тощо) змінювати свою структуру і властивості. Процес порушення природної структури білків, який супроводжується розгортанням білкової молекули без зміни її первинної структури, називають денатурацією. Здебільшого денатурація необоротна. Але якщо на початкових стадіях денатурації припиняється дія чинників, що призвели до неї, білок може відновити свій початковий стан. Це явище називають ренатурацією. У живих організмів оборотна денатурація часто пов’язана з виконанням певних функцій білковими молекулами: забезпеченням рухів, передачею до клітини сигналів з навколишнього середовища, прискоренням біохімічних реакцій тощо. Необоротний процес руйнування первинної структури білків називають деструкцією. ІV. Осмислення об‘єктивних зв’язків та взаємозалежностей у вивченому матеріалі. Виконання лабораторної роботи “Вивчення властивостей ферментів”. V. Узагальнення та систематизація знань.  1. Робота з таблицею «Просторова конфігурація білків» 2. Робота з підручником. Знайти відповіді на запитання: - які хімічні елементи входять до складу білків? - якого хімічного елемента найбільше у білках? - яких елементів порівняно небагато у білках? VІ. Підведення підсумків уроку. VІІ. Надання та пояснення домашнього завдання. Урок 4 Макромолекули: нуклеїнові кислоти, їхня будова, властивості, функції. Мета. Освітня. Розширити знання учнів про природні біополімери; ознайомити із будовою, властивостями та функціями нуклеїнових кислот; розкрити значення цих органічних сполук у живій природі. Розвиваюча. Розвивати уміння порівнювати будову та функції органічних молекул та сполук у клітинах живих організмів; уміння спостерігати, аналізувати та робити відповідні висновки. Виховна. Виховувати матеріалістичні погляди та уявлення про спадковий зв’язок живої і неживої природи на основі єдності хімічного складу. Тип уроку. Засвоєння нових знань. Форма уроку. Синтетична. Місце уроку в навчальній темі. Поточний. Методи і методичні прийоми: 1.Інформаційно- рецептивний: а) словесний: розповідь-пояснення, опис, бесіда, повідомлення учнів, робота з підручником. б) наочний: ілюстрація, демонстрація. Прийоми навчання: виклад інформації, пояснення, активізація уваги та мислення, одержання з тексту та ілюстрацій нових знань. 2. Репродуктивний. Прийоми навчання: подання матеріалу в готовому вигляді, конкретизація і закріплення вже набутих знань. 3. Проблемно - пошуковий: постановка проблемного питання. Прийоми навчання: постановка взаємопов’язаних проблемних запитань, активізація уваги та мислення. 4.Релаксопедичний: психологічне розвантаження. Міжпредметні зв ́язки: хімія, фізика, географія. Матеріали та обладнання: малюнки, таблиці, муляж ДНК. Основні поняття та терміни: оганічні сполуки, полімери, біополімери, мономери, нуклеотид, нуклеус, нуклеїнові кислоти: рибонуклеїнова та дезоксирибонуклеїнова, мікробіологія. ХІД УРОКУ І. Актуалізація опорних знань та чуттєвого досвіду учнів. Охарактеризувати функції білків: будівельну, транспортну, рухову, сигнальну, енергетичну, захисну, регуляторну… Що буде у результаті досліду: у пробірку з розчином білка долити краплинками розчину мідного купоросу (при цьому утворюється осад у вигляді пластівців). ІІ. Мотивація навчально-пізнавальної діяльності учнів. Повідомити тему, мету та завдання уроку. ІІІ. Сприймання та засвоювання учнями нового матеріалу. Нуклеїнові кислоти – природні високомолекулярні органічні сполуки, що забезпечують збереження і передавання спадкової інформації в організмі.Це – складні високомолекулярні біополімери, мономерами яких є нуклеотиди. Число нуклеотидів у складі однієї молекули нуклеїнової кислоти може становити від 200 до 200 млн. Уперше нуклеїнові кислоти виявили в ядрі клітин, звідки й походить назва цих сполук (від лат. нуклеус – ядро). Але згодом ці сполуки виявили і в інших частинах клітини. Молекула нуклеотиду складається з трьох частин: залишківнітратної основи, п’яти-вуглецевого моносахариду (пентози) та ортофосфатної кислоти. Залежно від виду пентози, що входить до складу нуклеотиду, розрізняють два типи нуклеїнових кислот: дезоксирибонуклеїнову (ДНК) і рибонуклеїнові (РНК). До складу ДНК входить залишок дезоксирибози, до РНК – рибози. У молекулах ДНК і РНК містяться залишки різних нітратних основ. У молекулі ДНК – залишки аденіну (скорочено позначається літерою А), гуаніну (Г), цитозину (Ц) та тиміну (Т), у молекулі РНК – аденіну (А), гуаніну (Г), цитозину (Ц) та урацилу (У). Три типи нітратних основ для молекул ДНК і РНК спільні (нуклеотиди з аденіном, гуаніном і цитозином), натомість тимін міститься лише в молекулах ДНК, тоді як урацил – тільки в молекулах РНК. Як і молекулам білків, молекулам нуклеїнових кислот притаманні різні рівні просторової організації (конформації). Мономерами нуклеїнових кислот є нуклеотиди. До складу кожного нуклеотиду входять: 3. азотна основа; 4. вуглевод; 5. залишок фосфорної кислоти. Будова ДНК. Молекули ДНК у клітинах еукаріотів містяться в ядрі, пластидах і мітохондріях, а прокаріотів – в особливих ділянках цитоплазми. Розшифрування структури ДНК має свою історію. 1950 року американський учений українського походження Ервін Чаргафф (1905–2002) та його колеги виявили певні закономірності кількісного вмісту нітратних основ у молекулі ДНК: - по-перше, кількість нуклеотидів, що містять аденін у будь-якій молекулі ДНК, дорівнює числу нуклеотидів, які містять тимін (А = Т), а число нуклеотидів з гуаніном – числу нуклеотидів з цитозином (Г = Ц); - по-друге, сума нуклеотидів з аденіном і гуаніном дорівнює сумі нуклеотидів з тиміном і цитозином (А + Г = Т + Ц). Це відкриття сприяло встановленню в 50-х роках ХХ ст. просторової структури молекули ДНК. Молекула ДНК складається з двох ланцюгів нуклеотидів, які сполучаються між собою за допомогою водневих зв’язків. Ці зв’язки виникають між двома нуклеотидами, які ніби доповнюють один одного за розмірами. Встановлено, що залишок аденіну (А) нуклеотиду одного ланцюга молекули ДНК завжди сполучається із залишком тиміну (Т) нуклеотиду іншого ланцюга (між ними виникає два водневі зв’язки), а гуаніну (Г) – з цитозином (Ц) (між ними виникає три водневі зв’язки). Чітка відповідність нуклеотидів у двох ланцюгах ДНК має назву комплементарність (від лат. комплементум – доповнення). При цьому два ланцюги нуклеотидів обвивають один одного, створюючи закручену вправо спіраль діаметром приблизно 2 нм [1 нм (нанометр )дорівнює 1 • 10–6 мм]. Так виникає вторинна структура молекули ДНК, тоді як первинна це певна послідовність залишків нуклеотидів, розташованих у вигляді подвійного ланцюга. При цьому окремі нуклеотиди сполучаються між собою в ланцюжок за рахунок особливого різновиду міцних ковалентних зв’язків, які виникають між залишком вуглевода одного нуклеотиду та залишком ортофосфатної кислоти іншого. Молекули ДНК у клітині становлять компактні структури. Наприклад, довжина ДНК найбільшої хромосоми людини дорівнює 8 см, але вона скручена таким чином, що вміщується в хромосомі завдовжки 5 мкм. Це відбувається завдяки тому, що дволанцюгова спіраль ДНК зазнає подальшого просторового ущільнення, формуючи третинну структуру – суперспіраль. Така будова характерна для ДНК хромосом еукаріотів і зумовлена взаємодією між ДНК та ядерними білками. У ядерній зоні клітин прокаріотів молекула ДНК має кільцеву будову. 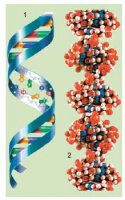 Властивості ДНК. Так само як і молекули білків, молекули ДНК здатні до денатурації та ренатурації, а також деструкції. За певних умов (дія кислот, лугів, високої температури тощо) водневі зв’язки між комплементарними нітратними основами різних ланцюгів молекули ДНК розриваються. При цьому молекула ДНК повністю або частково розпадається на окремі ланцюги й відповідно втрачає свою біологічну активність. Після припинення дії негативних чинників структура молекули може відновлюватися завдяки поновленню водневих зв’язків між комплементарними ну- клеотидами. Важлива властивість молекул ДНК – їхня здатність до самоподвоєння. Це явище ще називають реплікацією. Воно ґрунтується на принципі комплементарності: послідовність нуклеотидів у новоствореному ланцюзі визначається їхнім розташуванням у ланцюзі материнської молекули ДНК. При цьому ланцюг материнської молекули ДНК слугує матрицею. Реплікація ДНК – напівконсервативний процес, тобто дві дочірні молекули ДНК містять по одному ланцюгу, успадкованому від материнської молекули, і по одному – синтезованому заново. Завдяки цьому дочірні молекули ДНК є точною копією материнської. Це явище забезпечує точну передачу спадкової інформації від материнської молекули ДНК дочірнім. Функції ДНК. Основні функції ДНК – це кодування, збереження та реалізація спадкової інформації, передача її дочірнім клітинам при розмноженні. Зокрема, окремі ланцюги молекули ДНК слугують матрицею для синтезу різних типів молекул РНК. Цей процес називається транскрипцією. Одиницею спадковості всіх організмів є ген – ділянка молекули ДНК (у деяких вірусів – РНК), який несе спадкову інформацію про структуру певного білка або нуклеїнової кислоти. Отже, саме ДНК кодує і зберігає спадкову інформацію в організмі і забезпечує її передачу дочірнім клітинам під час поділу материнської. Функціонально ген – цілісна одиниця спадковості, бо будь-які порушення його будови змінюють закодовану в ньому інформацію або призводять до її втрати. Типи РНК. Молекули РНК клітин прокаріотів та еукаріотів складаються з одного ланцюга. Існують три основні типи РНК, які відрізняються за місцем розташування у клітині, розмірами та функціями. 1.Інформаційна, або матрична, РНК (іРНК, або мРНК) становить собою копію певної ділянки молекули ДНК. Така молекула переносить спадкову інформацію від ДНК до місця синтезу поліпептидного ланцюга, а також бере безпосередню участь у його збиранні. 2.Транспортна РНК (тРНК) має найменші розміри серед усіх молекул РНК (складається з 70–90 нуклеотидів). Вона приєднує амінокислоти і транспортує їх до місця синтезу білкових молекул. Там молекула тРНК «впізнає» відповідну ділянку іРНК. Ця ділянка – послідовність з трьох нуклеотидів, яка кодує одну з амінокислот. Таким чином визначається порядок розташування амінокислотних залишків у молекулі білка, що синтезується. Кожну з амінокислот транспортує до місця синтезу білка певна тРНК. У транспорті комплексу «молекула тРНК–залишок амінокислоти» беруть участь мікротрубочки та мікронитки цитоплазми. Транспортна РНК може мати вторинну структуру, що за формою нагадує листок конюшини. Така структура зумовлена тим, що в певних ділянках молекули тРНК (4–7 послідовних ланок) між комплементарними ну- клеотидами виникають водневі зв’язки. Біля верхівки «листка» містяться три нуклеотиди, або триплет, який за генетичним кодом відповідає певній амінокислоті. Цей триплет називають антикодоном. Біля основи молекули ДНК є ділянка, до якої завдяки ковалентному зв’язку приєднується відповідна амінокислота. Молекула тРНК може утворювати і складнішу конформацію (третинну), що нагадує латинську літеру «L» або слов’янську «Г». 3.Рибосомна РНК (рРНК) входить до складу особливих органел клітини – рибосом. Разом з білками вона виконує структурну функцію, забезпечуючи певне просторове розташування іРНК й тРНК під час біо синтезу білкової молекули. У клітинах еукаріотів рРНК синтезується в ядерці. ІV. Осмислення об‘єктивних зв’язків та взаємозалежностей у вивченому матеріалі. Робота з таблицею та зі схемами. 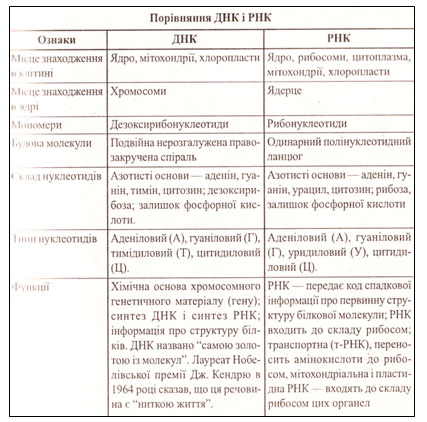 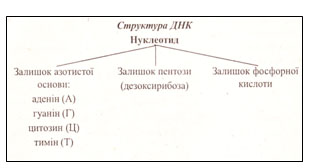 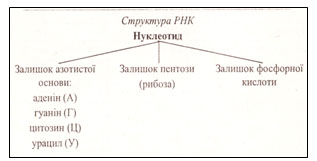 V. Узагальнення та систематизація знань. Значення нуклеїнових кислот. VІ. Підведення підсумків уроку. VІІ. Надання та пояснення домашнього завдання. Приготувати повідомлення про вміст хімічних сполук у різних видів організмів. Урок 5 Єдність хімічного складу організмів. Мета. Освітня. Систематизувати знання учнів про неорганічні та органічні речовини живих організмів та спільність їхніх елементів. Розвиваюча. Розвивати уміння порівнювати різноманітні сполуки та їх значення у житті організмів; уміння визначати співвідношення цих елементів у живій та неживій природі. Виховна. Виховувати бережливе ставлення до життєвих процесів, які відбуваються в живих організмах та власному організмі. Підвести учнів до висновку про єдність неживої і живої природи на основі єдності хімічного складу організмів. Тип уроку. Систематизація знань учнів. Форма уроку. Синтетична. Методи і методичні прийоми: 1. Інформаційно- рецептивний: а) словесний: бесіда, повідомлення учнів; б) наочний: ілюстрація, демонстрація, ТЗН. Прийоми навчання: виклад інформації, пояснення, активізація уваги та мислення. 2.Репродуктивний. Прийоми навчання: подання матеріалу в готовому вигляді, конкретизація і закріплення вже набутих знань. 3. Проблемно - пошуковий: постановка проблемного питання. Прийоми навчання: постановка взаємопов’язаних проблемних запитань, активізація уваги та мислення. 4.Сугестивний: застосування різних видів мистецтва. 5.Релаксопедичний: психологічне розвантаження. Міжпредметні зв ́язки: хімія, географія, образотворче мистецтво. Матеріали та обладнання: схеми, малюнки. Основні поняття та терміни: з усіх попередніх уроків. ХІД УРОКУ І. Актуалізація опорних знань та чуттєвого досвіду учнів. Повторення знань про хімічні елементи таблиці Д.Мендєлєєва та кількісний склад певних елементів у живій природі, тобто поділ їх на органогенні, мікроелементи та мікроелементи. Експрес-методом з’ясувати знання про неорганічні та органічні сполуки живих організмів. ІІ. Мотивація навчально-пізнавальної діяльності учнів. Поставити за мету, що єдність живої речовини – це нерозривна молекулярно-біохімічна єдність, єдине ціле з характерними для кожної геологічної епохи рисами. ІІІ. Сприймання та засвоювання учнями нового матеріалу. Повідомлення учнів про: - вміст неорганічних та органічних сполук у різних видів організмів; - вміст хімічних елементів у земній корі, морській воді, рослинах і тваринах; - вміст хімічних сполук безпосередньо в організмі людини. Повідомлення учнів про значення в організмах елементів та сполук (завдання було задане на попередніх уроках). - Ферум входить до складу гемоглобіну крові, за його нестачі розвивається недокрів’я. На нього багаті: м’ясо тварин, риба, абрикоси, червоний виноград, селера, у молочних продуктах його майже немає. - Кальцій потрібний для формування скелету, для зсідання крові, без нього не було б зубів. Найбільше його у полуницях, смородині, черешні, селері та молочних продуктах. - Натрій впливає на процеси травлення, тиск крові, кількість води в організмі. Головним джерелом цього елемента є кухонна сіль. Щорічно людина з’їдає 7-9 кг солі, а за життя – 500 кг. - Йод сприяє нормальній роботі щитоподібної залози. За його нестачі розвивається зоб. Джерелом йоду є морепродукти та йодована сіль. - Фосфор важливий для кісток, зубів, впливає на роботу серця, нирок, нервових клітин, деяких ферментів. Велика його кількість міститься у ягодах, горіхах, капусті, моркві, рибі. - Ліпіди. Найважливішими джерелами тваринних жирів у нас є сало, потім вершкове масло та жири риб. У кулінарії використовують ще саломас. Серед рослинних жирів найбільше вживається соняшникова, кукурудзяна та оливкова олії. У результаті окиснення 1 г жиру вивільняється близько 40 кДж енергії, а продуктом окиснення є вода. Із 100 г жиру утворюється 110 води. - Вуглеводи. Найпоширеніші моносахариди, дисахариди та полісахариди. Моносахариди – головне джерело енергії в клітині: розщеплення 1г глюкози дає 17,2 кДж енергії. З моносахаридів утворюються полісахариди, залишки моносахаридів входять до складу нуклеїнових кислот, амінокислот, ліпідів та білків. Попарно сполучені моносахариди утворюють дисахариди. Найбільш важливим є сахароза, молекули якої утворені залишками глюкози та фруктози. Коренеплоди цукрових буряків здатні накопичувати до 25% сахарози. Деякі мікроорганізми використовують сахарозу для спиртового, маслянокислого, молочнокислого бродіння. Дисахарид мальтоза складається із двох залишків глюкози. Мальтоза – проміжний продукт розщеплення полісахаридів утворюється під час виробництва пива та вина. Молоко містить молочний цукор – лактозу. Цей вуглевод є унікальним джерелом енергії для немовлят. До полісахаридів належать крохмаль, целюлоза, хітин. Крохмаль відкладається у бульбах картоплі, зернах злакових рослин. У харчовій промисловості крохмаль розщеплюють до глюкози. Целюлоза – полісахарид, який використовують для виготовлення паперу і тканин. Покриви членистоногих утворені з хітину. Він входить ще до складу клітинних стінок грибів. - Білки. Чому назва білки. Вважають від того, що вони здатні біліти під час нагрівання. Мономерами є 20 амінокислот та 4 структури. Під час термічної обробки або підвищеної кислотності (скисання молока), молекули білка втрачають свою структуру – це так звана денатурація. У молоці міститься розчинний білок казеїноген, який у шлунку під дією хлоридної кислоти та ферментів денатурує і перетворюється на нерозчинний білок казеїн. Цікаво, що у клітинах шлунково-кишкового тракту виробляються білки, що спричиняють поганий настрій. Особливо характерно це для чоловіків, тож недарма кажуть, що шлях до серця чоловіків лежить через шлунок. Білки виконують цілу низку функцій: структурну, рухову, захисну, транспортну, живильну, регуляторну… - Нуклеїнові кислоти – ДНК та РНК мають велике значення в живих організмах. Без них жодна жива істота не могла б відтворити собі подібних. ІV. Осмислення об‘єктивних зв’язків та взаємозалежностей у вивченому матеріалі. Із різноманітної кількості наданих учнями картинок рослин і тварин погрупувати їх згідно наявності певних неорганічних та органічних сполук: - по кількості води; - по кількості певних мінеральних солей; - по кількості білків; - по кількості вуглеводів; - по кількості ліпідів. V. Узагальнення та систематизація знань. Поміркувати! Чи може знищення на планеті деяких хімічних речовин або їхній надлишок призвести до порушення природної рівноваги, що веде за собою різкі зміни молекулярно-біохімічних властивостей живої речовини і неможливість існування видів, у тому числі й людини? VІ. Підведення підсумків уроку. VІІ. Надання та пояснення домашнього завдання. Подібні публікації:
|
||||||||||||
Корисна інформація ↓
|
Реклама ↓
На сайті знайшли ↓
|
|||||||||||